서 론
오리고기는 우수한 동물성 단백질 공급원이자 높은 소화율로 그 소비가 꾸준히 증가하고 있는 축산식품 중 하나이다(Chang and Han, 2025; Kim et al., 2025a). 오리고기는 리놀렌산, 아라키돈산 등 불포화 지방산의 함량이 포화 지방산 보다 높다고 알려져 있으며, 이러한 불포화 지방산의 섭취는 혈액 콜레스테롤과 관련하여 건강에 이로운 영향을 준다는 연구들이 보고되고 있어 그 소비는 꾸준히 증가될 것으로 사료된다(Kang et al., 2014; Kim et al., 2025b).
그러나 오리고기는 도축 과정부터 생산, 가공, 포장 및 유통에 이르기까지 다양한 단계에서 Escherichia coli 및 Salmonella spp.와 같은 분변성 미생물에 의한 위해성은 지속적으로 보고되어 왔다(Laranja et al., 2021; Lee et al., 2023a). 이는 오리의 사육 및 도축 특성상 장내 미생물이 도축 과정 중 도체 표면으로 쉽게 전이될 수 있기 때문이다(Mazengia et al., 2015). 이러한 초기 미생물 오염은 이후 공정에서 교차오염으로 확대될 수 있어, 도축 공정 중 세척 단계는 도체 표면의 분변성 미생물을 저감하고 위생 수준을 확보하기 위한 핵심 관리 단계로 작용한다. 전 세계적으로 가장 보편적으로 사용되는 살균소독제는 염소계 용액(예: NaOCl, HOCl 등)으로, 일반적으로 50~200 ppm 농도로 희석하여 세척수로 적용되고 있다. 그러나 염소계 용액은 유기물과 반응할 경우 트리할로메탄(trihalomethane)과 같은 발암성 부산물을 생성할 가능성이 있어 식품 안전 측면에서 우려가 제기되고 있다(Lin et al., 2023). 이에 따라 화학적 위해성 없이 미생물학적 안전성을 확보할 수 있는 대체 살균 기술 개발의 필요성이 증가하고 있다. 이러한 배경에서 최근 도축 공정 중 세척 단계에서 유기산(젖산, 아세트산, 구연산 등)을 적용하고자 하는 연구들이 다수 보고되고 있다(Seok et al., 2021; Lee et al., 2023a). 유기산은 pH 저하를 통해 미생물 세포막 투과성을 증가시키고, 세포 내 대사 교란을 유도함으로써 병원성 미생물의 생존을 억제하는 장점을 가진다(Sampath et al., 2024). 유기산 중 특히 구연산은 식품 등급 물질로서 안전성이 높고, 잔류 독성에 대한 우려가 적어 도체 세척수로의 활용 가능성이 지속적으로 검토되어 왔다(Osazuwa et al., 2024). González-Fandos et al.(2009)은 가금육에 1~3% 구연산을 처리할 경우, 저장 중 총 호기성 미생물과 Listeria monocytogenes의 증식이 억제됨을 보고하였다. 또한 미국 식품의약국(U.S. Food and Drug Administration, FDA) 등 일부 국가의 규제 체계에서는 구연산을 포함한 식품 등급 유기산을 일반적으로 안전한 물질(Generally Recognized as Safe, GRAS)로 인정하여, 도체 세척용 항균제로 사용을 허용하고 있다(Jyung et al., 2023). 그러나 이러한 유기산 기반 세척은 단독 적용 시 미생물 저감 효과가 제한적이며, 실질적인 살균 수준(log reduction)이 미미하다는 한계가 지적되고 있다.
한편, 신선육을 포함한 다양한 식품의 세척 공정에 적용 가능한 대체 기술로서 플라즈마 처리수(plasma-treated water)가 최근 주목받고 있다(Tang et al., 2025). 플라즈마는 고체, 액체, 기체에 이은 물질의 제4상태로, 기체가 외부 에너지를 흡수함에 따라 이온, 전자 및 중성 입자 등이 공존하는 전기적으로 활성화된 상태를 의미한다. Plasma-treated water는 이러한 플라즈마를 물에 적용하여 제조된 용액으로, 플라즈마 방전 과정에서 생성된 다양한 활성종이 물 분자와 상호작용함으로써 과산화수소(hydrogen peroxide, H2O2), 질산염(nitrate, NO3−), 아질산염(nitrite, NO2−), 퍼옥시나이트러스산(peroxynitrous acid, ONOOH) 등과 같은 활성산소종(reactive oxygen species, ROS) 및 활성질소종(reactive nitrogen species, RNS)을 형성한다(Hadinoto et al., 2023). 이와 동시에 처리수의 pH는 감소하며, 생성된 활성종과 산성화된 환경은 미생물 제어에 기여하여 세척수로서의 잠재적인 살균 효과를 나타내는 것으로 보고되고 있다(Hadinoto et al., 2023; Tang et al., 2025).
최근에는 플라즈마를 유기산 용액에 적용함으로써 반응성 물질의 생성량과 안정성을 증가시키고, 이를 통해 살균 효과를 극대화하고자 하는 연구들이 보고되고 있다(Jyung et al., 2023; Lee et al., 2023a). 플라즈마 처리 유기산은 유기산에 의한 산성 환경과 플라즈마 방전으로 생성된 반응성 종이 복합적으로 작용함으로써, 기존 유기산 처리에 비해 보다 강화된 미생물 제어 효과를 나타낼 가능성이 제시되고 있다(Lee et al., 2023a). Jyung et al.(2023)은 유기산에 비해리형(protonated form) 특성이 단순 확산(simple diffusion)을 통해 세포막을 통과하여 세포 내 pH를 감소시키고, 그 결과 catalase(CAT), superoxide dismutase(SOD), glutathione peroxidase(GPx)와 같은 ROS 제거 효소의 활성을 저해함으로써, 플라즈마 또는 plasma-treated water에 의해 생성된 다양한 활성종이 미생물 세포를 보다 효과적으로 공격하여 살균효과를 높일 수 있다고 보고하였다. 또한 이러한 복합 처리는 경제성과 적용성이 우수한 유기산의 장점을 유지하면서도, 단독 사용 시 살균 효과가 제한적인 플라즈마 처리의 한계를 보완함으로써, 보다 높은 수준의 미생물 제어 효과를 달성하고 산업적 활용 가능성을 확장할 수 있을 것으로 판단된다. 그러나 현재까지 보고된 연구들 중 구연산에 플라즈마를 처리한 연구는 제한적이며, 특히 가금류를 대상으로 두 기술의 복합 처리 효과를 평가한 연구는 부족한 실정이다. 또한, 이러한 복합 기술을 가금류 도체의 세척 공정에 적용하기 위한 세척수 활용 가능성에 대한 검증 역시 미흡한 상황이다.
따라서 본 연구에서는 오리 도축 공정에 적용 가능한 세척수의 살균 가능성을 평가하기 위하여, 오리 껍질을 시료로 하여 물(water), 구연산수(citric acid), plasma-treated water, 그리고 플라즈마 처리 구연산수(plasma-treated citric acid)를 각각 적용하였다. 이를 통해 각 세척수가 오리 껍질 내 E. coli O157:H7 및 S. enteritidis의 살균 효과를 확인하고, 동시에 오리 껍질의 품질 특성 변화를 평가하고자 하였다.
재료 및 방법
본 연구에서 사용된 오리 껍질 시료는 다미축산(충북, 한국)에서 구매하여 사용하였다. 오리 껍질은 무균 작업대에서 10 g씩 소분하였다. 살균 실험에 사용할 오리 껍질 시료 표면의 잔존미생물 제거를 위해 70% 에탄올로 표면을 1차 세척을 한 후 살균에 영향을 미칠 수 있는 에탄올 제거를 위해 멸균 증류수로 2차 세척하였다. 이후 무균 작업대에서 오리 껍질 양쪽 면을 5분씩 UV 처리하였다. 품질 실험에 사용할 오리 껍질 시료는 별도의 세척 과정을 거치지 않았다.
본 연구에서 사용한 E. coli O157:H7(NCCP 1771, National Culture Collection for Pathogens, Korea)와 S. enteritidis (NCCP 14771, National Culture Collection for Pathogens, Korea)는 −80°C에서 보관 중인 균주를 사용하였다. 각 시험 균주는 25 mL의 tryptic soy broth(TSB, MB cell, Korea)와 nutrient broth(NB, MB cell, Korea)에 각각 접종하여 37°C에서 48시간 동안 배양하였다. 배양된 시험균주는 원심분리기(1580R; Labogene, Gyrozen Co., Ltd., Korea)를 이용하여 4°C, 3600×g 조건으로 20분간 원심분리하였다. 침강된 펠렛을 0.85% 멸균 생리식염수에 현탁하여 최종 약 8~9 log colony-forming unit(CFU)/mL의 세균 현탁액을 제조하였다. 각각의 세균 현탁액은 살균 실험용 오리 시료에 100 µL씩 점접종(spot inoculation)을 하고 멸균 스프레더(spreader)를 이용하여 문지른 후 무균 작업대에서 2차 오염을 방지하며 미생물이 표면에 잘 부착되도록 10분 동안 건조하였다. 또한, 품질 실험용 오리 껍질 시료는 접종 과정을 거치지 않았다.
본 실험에서는 서로 다른 4개의 세척수(water, citric acid, plasma-treated water, 그리고 plasma-treated citric acid)를 제조하여 실험에 사용하였다. 이후 세척수의 살균력을 평가하기 위해 오리 껍질(10 g)을 각 세척수(300 mL)에 3분간 담가 평가하였다. Citric acid는 시중에서 구입한 무수 구연산(100%, RZBC Group Co., Ltd., China)을 멸균 증류수에 용해하여 최종 농도 3%(w/v)가 되도록 제조하였다.
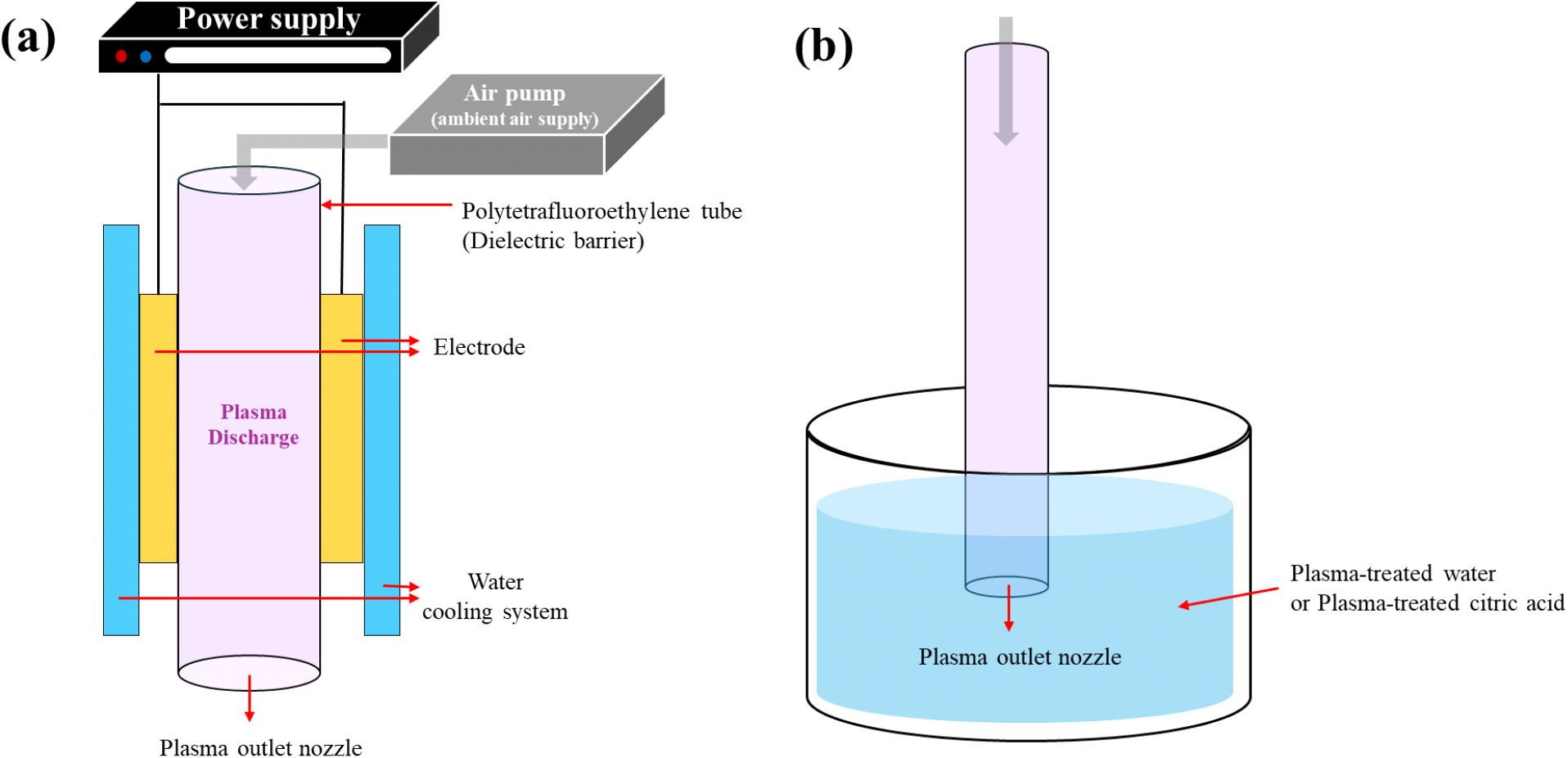
플라즈마 처리는 DBD(dielectric barrier discharge) 방식의 저온 플라즈마 발생 장치(Plasmapp Co., Ltd., Korea)를 사용하여 수행하였다(Fig. 1). 플라즈마 발생을 위해 질소와 산소를 포함한 대기 중 공기를 주입 가스로 사용하였으며, 방전 조건은 1.5 kW와 60 kHz로 설정하였다. Plasma-treated water 및 plasma-treated citric acid는 각각 water와 citric acid 300 mL에 플라즈마 발생 장치를 통해 생성된 플라즈마 가스를 유리관을 통해 3분간 주입하는 방식으로 제조하였다.
각각의 세척수 세척 후, 오리 껍질(10 g)은 멸균 샘플 백(3M, USA)에 0.85% 멸균 생리식염수(90 mL)와 함께 넣고 stomacher(BagMixer®400, Interscience, France)를 이용하여 균질하였다. 균질화된 시료는 각각 eosin methylene blue agar(EMB, MB cell, Korea)와 xylose lysine deoxycholate agar(XLD, MB cell, Korea)에 도말하여 E. coli O157:H7과 S. enteritidis 수를 확인하였다. 배지는 37°C에서 24시간 동안 배양하였으며, 배양 후 배지 위에 형성된 균체(colony)를 계수하여 log CFU/g으로 나타내었다.
세척수 및 오리 껍질의 pH는 보정된 pH meter(PM-3; CAS Co., Ltd., Korea)를 사용하여 측정하였다. 세척수의 pH는 제조 직후 측정을 진행하였으며, 오리 껍질 시료의 pH는 시료 1 g에 증류수 9 mL를 혼합한 후 균질기(T10 basic ULTRA-TURRAX; IKA GmbH & Co., Germany)를 이용하여 균질한 후 원심분리기(1580R; Labogene, Gyrozen Co., Ltd., Korea)를 이용하여 4°C, 3,100×g 조건으로 10분간 원심분리한 후, 상층액을 여과한 시료를 측정하였다.
오리 껍질 시료의 색도 특성은 색차계(CM-5; Konica Minolta, Japan)를 이용하여 측정하였으며, 측정 구역은 8 mm로 설정하여 측정하였다. 색도값은 명도(lightness, L*), 적색도(redness, a*) 및 황색도(yellowness, b*)로 나타내었다.
오리 껍질 시료의 지질 과산화 정도는 TBARs 분석법을 통해 MDA(malondialdehyde) 농도를 측정하였다. 분석은 Yong et al.(2023)이 제시한 분광광도법(spectrophotometric method)을 오리 껍질 시료에 맞게 일부 수정하여 적용하였다. 각각의 오리 껍질 샘플 5 g과 3차 증류수 15 mL를 넣고 혼합한 후 7.2% butylated hydroxytoluene 용액 50 µL 첨가하였다. 이후 9,000×g 조건으로 30초간 균질한 후, 균질화된 시료 2 mL에 20 mM thiobarbituric acid/15% trichloroacetic acid 용액 4 mL를 첨가하였다. 혼합 시료는 90°C에서 30분간 반응시켰다. 이후 시료는 10분간 냉각한 후, 4°C, 2,300×g 조건으로 15분간 원심 분리하였다. 이후, 상등액을 분광광도계(Varioskan Lux; Thermo Fisher Scientific, MA, USA)를 이용하여 532 nm에서 흡광도를 측정하였다. MDA 농도는 1,1,3,3-tetraethoxypropane을 이용하여 작성된 표준 곡선에 준하여 산출하였으며, TBARs 값은 MDA 농도를 기준으로 mg MDA/kg 단위로 나타내었다.
결과 및 고찰
Table 1은 water, citric acid, plasma-treated water, 그리고 plasma-treated citric acid를 세척수로서 오리 껍질을 3분간 세척하였을 때 E. coli O157:H7 및 S. enteritidis의 생균수 변화를 나타낸 것이다. 세척 전 오리 껍질 내 E. coli O157:H7과 S. enteritidis의 초기 균수는 각각 5.80 및 6.34 log CFU/g이었다. Water로 세척된 오리 껍질에서는 E. coli O157:H7과 S. enteritidis의 생균수가 각각 0.45 및 0.48 log CFU/g 감소하여 세척 전과 비교해 유의적인 감소를 보였다(P<0.05). 이는 세척 과정에서 오리 껍질 표면에 부착된 미생물이 물리적으로 제거되어 나타난 결과로 판단된다. Citric acid로 세척한 오리 껍질 내 E. coli O157:H7 및 S. enteritidis 수는 세척 전과 비교하여 각각 2.48 및 2.77 log CFU/g만큼 유의적으로 감소하였다(P<0.05). 반면, plasma-treated water로 세척한 오리 껍질 내 E. coli O157:H7 및 S. enteritidis 수는 세척 전과 비교하여 각각 0.93 및 0.92 log CFU/g 유의적으로 감소하여 citric acid로 세척된 오리 껍질보다 유의적으로 낮은 수준의 세척 후 미생물 불활성화 효과를 나타내었다(P<0.05). 주목할 만한 점은 plasma-treated citric acid로 세척된 오리 껍질 내 두 균수가 모두 검출한계 이하로 감소하여 가장 높은 미생물 불활성화 효과를 나타내었다(P<0.05).
Control: Unwashed.
본 연구에서 사용된 세척수는 생성 과정에서 pH 감소 및 다양한 화학종의 형성이 발생할 수 있으며, 이러한 변화는 미생물의 불활성화에 영향을 미칠 가능성이 있다. 따라서 각 세척수 제조 직후 pH를 측정하였다. Fig. 2에 제시된 바와 같이, 본 연구에서 사용된 세척수의 제조 직후 pH는 water의 pH가 7.17로 가장 높게 나타났으며, plasma-treated water(2.87), citric acid(1.84) 그리고 plasma-treated citric acid (1.76) 순으로 유의적으로 낮은 값을 보였다(P<0.05). 이러한 pH 차이는 각 세척수의 미생물 불활성화 효과와 밀접한 관련이 있는 것으로 판단된다.
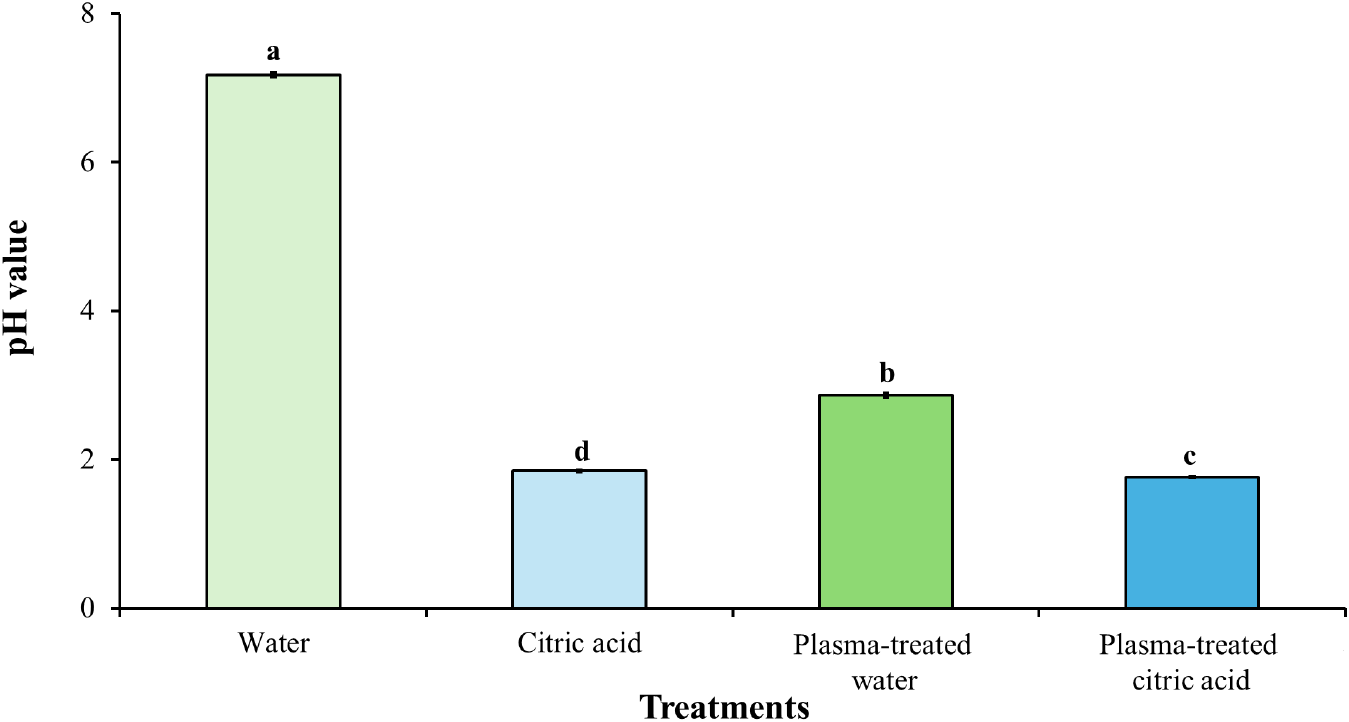
구연산은 약산성 유기산으로서, 물에 용해될 경우 세 개의 카르복실기(COOH)에서 수소이온(H+)이 단계적으로 해리되면서 용액 내 수소이온 농도가 증가하고 결과적으로 pH가 감소한다(Mudunkotuwa and Grassian, 2010). 본 연구에서 water에 구연산을 3% 첨가한 citric acid의 pH는 7.17에서 1.84로 water와 비교하여 유의적으로 감소하였다(P<0.05). 이러한 구연산에 의한 감소된 citric acid의 pH는 세포막 손상 및 세포 내 효소 활성 저해와 같은 산성 스트레스를 유도하며 미생물의 사멸을 유도할 수 있다(Jin and Kirk, 2018). Mani-López et al.(2012)은 구연산과 같은 유기산이 그람 음성균의 외막(outer membrane) 투과성을 증가시키고 외막으로부터 지질다당류(lipopolysaccharide, LPS)를 유리시켜 미생물의 사멸을 유도할 수 있다고 보고하였다. 또한 유기산은 비해리형으로써 단순 확산을 통해 세포막을 통과하여 세포질로 유입된 후, 미생물의 세포 내에서 해리되어 양성자를 생성함으로써 세포 내 pH를 감소시키고, 그 결과 catalase, superoxide dismutase, glutathione 및 peroxidase와 같은 ROS 제거 효소의 활성을 저해하여 미생물이 ROS의 산화적 공격에 더욱 취약해질 수 있으며 궁극적으로 미생물의 사멸을 유도할 수 있다(Jyung et al., 2023). Lee et al.(2023)은 구연산을 0.5 및 1% 첨가한 처리수를 이용하여 돼지 등심에 처리하였을 때 구연산의 농도가 높아질수록 더 낮은 pH를 나타냄과 동시에 높은 E. coli O157:H7과 S. typhimurium의 불활성화 효과를 나타냈다고 보고하였다. Burel et al.(2021)은 구연산의 첨가 농도에 따라 pH 감소 정도가 달라지며, 이와 같은 최종 pH는 미생물 불활성화에 중요한 영향을 미친다고 보고한 바 있다.
Plasma-treated water의 경우, 플라즈마 활성종이 물분자와 상호작용하는 과정에서 생성된 H2O2, NO3−, NO2−, ONOOH와 같은 활성종과 낮은 pH에 의해 미생물이 불활성화된 것으로 판단된다. 본 연구에서 plasma-treated water는 citric acid 및 plasma-treated citric acid와 비교하여 유의적으로 낮은 E. coli O157:H7과 S. typhimurium 불활성화 효과를 나타내었다(P<0.05). 이러한 결과는 plasma-treated water가 citric acid와 비교하였을 때 유의적으로 높은 pH(2.87)를 나타내었고, 다양한 유기물이 존재하는 오리 껍질 환경으로 인해 불활성화 효과가 제한적으로 나타난 것으로 판단된다. 이는 plasma-treated water 내 존재하는 다양한 활성종들이 미생물뿐만 아니라 주변의 유기물과도 경쟁적으로 반응함으로써, 실제 미생물에 도달하는 활성종의 양이 감소하고 그에 따라 불활성화 효율이 저하될 수 있다는 기존 연구 결과와도 일치한다(Baek et al., 2020). 또한, 그람 음성균이 보유한 세포벽 내 외막과 LPS 구조는 활성종의 세포 내 침투를 물리·화학적으로 제한하여 plasma-treated water 세척 효과를 저감시켰을 가능성도 배제할 수 없다. 특히, 얇은 펩티도글리칸 층을 갖는 그람 음성균이 직접 플라즈마 처리에서는 상대적으로 낮은 저항성을 보인다는 기존 보고와 달리, plasma-treated water의 경우에는 물리적 손상 효과(physical etching)가 존재하지 않고 용액 내 화학적 활성종에 의한 살균 작용에 의존한다는 점에서 차이를 보인다. 이러한 특성으로 인해, 그람 음성균의 외막과 같은 세포벽 구조적 특성 역시 plasma-treated water의 제한적인 미생물 불활성화 효과에 기여할 수 있었을 것으로 해석된다(Mai-Prochnow et al., 2021).
반면, plasma-treated citric acid는 citric acid에 의해 형성된 강한 산성 환경과 플라즈마 처리 과정에서 생성된 다양한 활성종이 복합적으로 작용함으로써, 두 균주 모두에 대해 가장 큰 수준의 생리적 스트레스를 유도한 것으로 판단된다. Lund et al.(2020)은 낮은 pH 환경이 plasma-treated water 단독 처리보다 병원성 세균의 세포 내 생화학적 시스템에 더 큰 스트레스를 유도한다고 보고하였으며, Lee et al.(2023b) 또한 plasma-treated citric acid가 낮은 pH, 향상된 산화환원전위(oxidation-reduction potential), 그리고 증가된 활성종 농도로 인해 plasma-treated water 단독 처리와 비교하여 향상된 미생물 불활성화 효과를 나타낸다고 보고한 바 있다. 또한 앞서 언급한 바와 같이, 유기산 처리로 인한 외막 투과성 증가와 세포 내 ROS 제거 효소 활성 저해가 plasma-treated water 내 활성종에 의한 산화적 스트레스를 더욱 증폭시켜, 제한된 plasma-treated water의 불활성화 효과를 유기산과의 복합효과를 통해 보다 높은 불활성화 효과를 나타낸 것으로 사료된다.
본 연구에서 각 세척수 세척 후 오리 껍질 내 E. coli O157:H7과 S. enteritidis의 불활성화 효과는 유사한 경향을 보였는데, 이는 두 균주가 모두 그람 음성균으로서 세포 구조 및 pH 민감도가 유사하기 때문으로 판단된다. Mai-Prochnow et al.(2021)은 세포벽의 구조에 따라 플라즈마에 의해 생성된 활성종에 따른 미생물의 불활성화 효과가 달라질 수 있다고 보고하였다. Suehr et al.(2020)은 E. coli와 Salmonella spp.의 생육 가능한 pH 범위를 각각 4.4~9.0과 3.8~9.5로 보고하였으며, 두 균주 모두 생육 가능한 pH보다 낮은 pH 환경에서도 일정 시간 생존할 수 있는 적응 기작을 보유하고 있어 유사한 pH 민감도를 가지고 있다고 보고한 바 있다. 본 연구에서 사용된 세척수의 주요 미생물 불활성화 요인은 낮은 pH와 플라즈마 활성종으로 판단되며, 이러한 조건에서 두 균주의 유사한 세포 구조와 pH 민감도가 유사한 오리 껍질 내 불활성화 효과를 나타난 것으로 사료된다.
Fig. 3은 각각의 세척수로 3분간 세척한 오리 껍질의 pH를 나타낸 것이다. 세척 전(control) 오리 껍질의 pH는 6.42였으며, water 세척 후에도 오리 껍질의 pH는 6.42로 유지되어 control과 비교하였을 때 유의적인 차이가 나타나지 않았다(P>0.05). 반면, citric acid, plasma-treated water 및 plasma-treated citric acid 세척된 오리 껍질의 pH는 각각 4.27, 3.52 및 3.50으로 세척 전 오리 껍질과 비교하였을 때 유의적으로 낮은 값을 보였다(P<0.05).
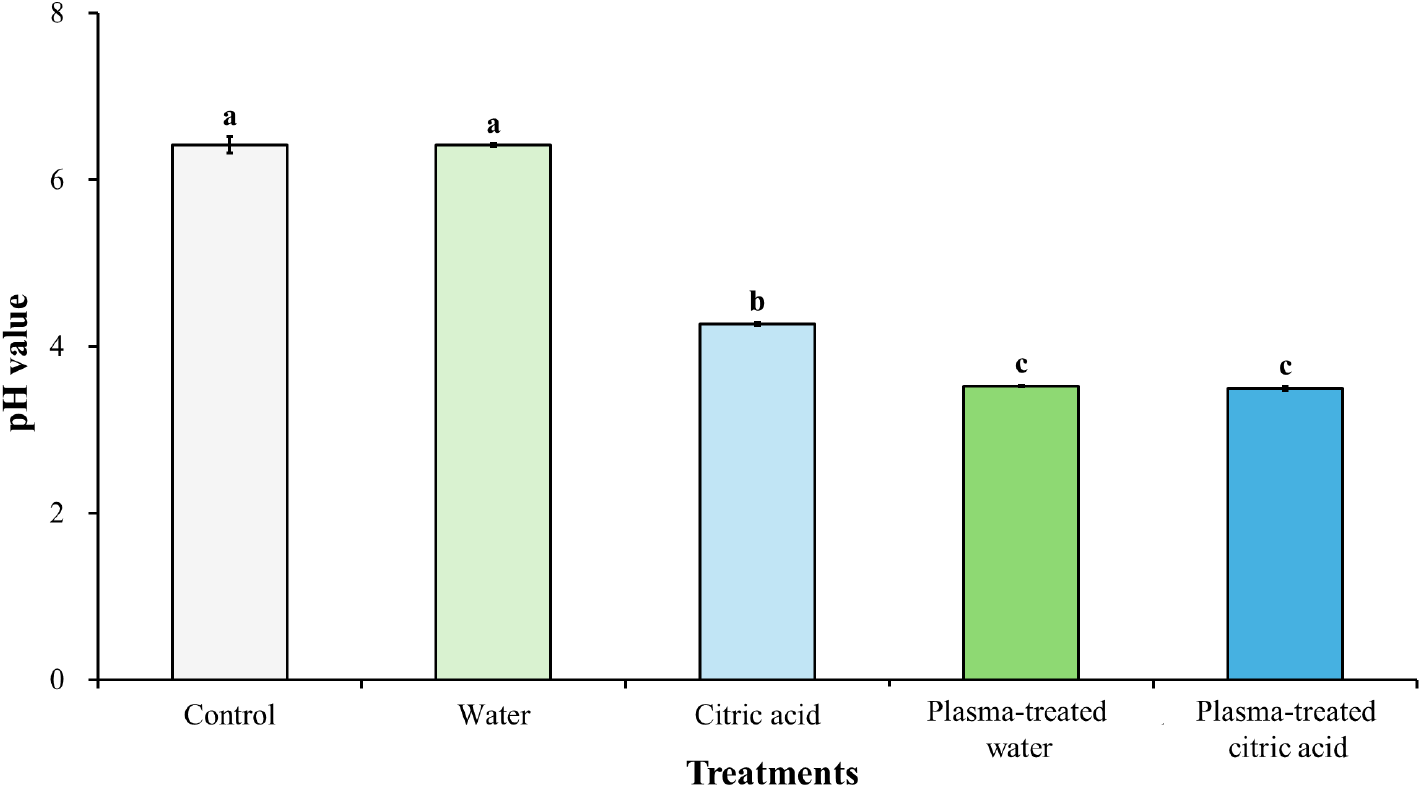
본 연구에서 citric acid 세척 후 오리 껍질의 pH는 4.27로, 세척 전과 비교하였을 때 유의적으로 낮은 값을 나타내었는데, 이러한 pH의 감소는 구연산이 수용액에서 해리되며 생성된 H+가 오리 껍질 표면 및 조직 내로 확산되어, 지질과 단백질의 산성화를 유도하고 결과적으로 조직 내 H+ 축적을 증가시킨 데 기인한 것으로 판단된다. Lee et al.(2023a)은 0.5% 구연산을 돼지 등심에 10분간 처리한 결과, pH가 5.82에서 5.32로 감소하였다고 보고하였다. 본 연구에서 관찰된 오리 껍질의 pH 변화는 6.42에서 4.27로 해당 연구보다 더 큰 감소 폭을 보였는데, 이는 적용된 구연산 농도가 3%로 상대적으로 높아 세척수의 pH가 더 낮았고, 이에 따라 오리 껍질 표면에 접촉·흡착되는 H+의 양이 증가하였기 때문에 더 높은 H+가 오리 껍질 내 축적되어 나타난 결과로 사료된다.
반면, Fig. 2에서 확인할 수 있다시피, plasma-treated water는 citric acid에 비해 pH가 높았음에도 불구하고, 세척 후 오리 껍질에서 유의적으로 더 큰 pH 감소를 유도하였다(P<0.05). 이는 plasma-treated water의 pH뿐만 아니라 plasma-treated water 내에 존재하는 다양한 반응성 활성종의 복합적인 작용에 기인한 결과로 판단된다. plasma-treated water에는 질산(nitric acid, HNO3) 및 아질산(nitrous acid, HNO2)을 포함한 다양한 활성종들이 존재하며, 이들은 수분과 상호작용하는 과정에서 NO2−와 NO3−로 해리되며 H+를 생성할 수 있다(Jeon et al., 2025). 이와 같이 생성된 H+가 오리 껍질 조직 내로 확산·축적되면서, 결과적으로 더 큰 폭의 pH 감소를 유도한 것으로 해석된다. 이와 유사하게 Yong et al.(2019)은 플라즈마 처리 후 돼지고기 육포(pork jerky) 내 잔존 NO2− 함량이 증가하였으며, 이에 동반된 H+ 농도 증가로 인해 pH가 유의적으로 감소하였다고 보고하였다.
주목할 점은 plasma-treated citric acid로 세척된 오리 껍질의 pH가 citric acid로 세척된 오리 껍질에 비해 유의적으로 낮게 나타났으나(P<0.05), plasma-treated water로 세척된 오리 껍질과 비교하였을 때 유의적인 차이를 보이지 않았다는 것이다(P>0.05). 이는 플라즈마 처리 유무에 따른 0.5% 구연산 처리 돼지 등심의 pH 차이가 유의적이지 않았다고 보고한 Lee et al.(2023)의 결과와 일치한다. 또한 Kang et al.(2022)은 0.8% 아세트산에 대해 30분간 플라즈마 처리를 수행한 후 닭 가슴살과 닭 다리살을 각각 10분간 처리하였을 때, 플라즈마 처리 유무에 따른 pH의 유의적인 차이가 나타나지 않았다고 보고하였다.
결론적으로 본 실험에서 사용된 세척수를 사용하여 오리 껍질을 세척하였을 때, 세척 전과 비교하여 유의적으로 pH가 감소되는 것을 확인하였다. 이러한 pH의 감소는 오리 껍질 내 지질 산화를 유도할 가능성이 존재한다. 이에 따라 본 연구에서는 세척 이후 오리 껍질의 품질 변화를 보다 종합적으로 평가하기 위해 지질 산화 정도에 대한 추가 분석을 수행하였다.
Fig. 4는 각각의 세척수로 오리 껍질을 3분간 세척한 후, 오리 껍질 내 지질 산화 정도를 TBARs 값으로 평가하여 나타낸 것이다. 오리 껍질의 TBARs 값은 control(0.08 mg MDA/kg)과 비교하여 plasma-treated water(0.16 mg MDA/kg) 및 plasma-treated citric acid(0.19 mg MDA/kg) 순으로 유의적으로 높게 나타났으며(P<0.05), water(0.08 mg MDA/kg) 및 citric acid(0.07 mg MDA/kg)는 유의적인 차이를 보이지 않았다.
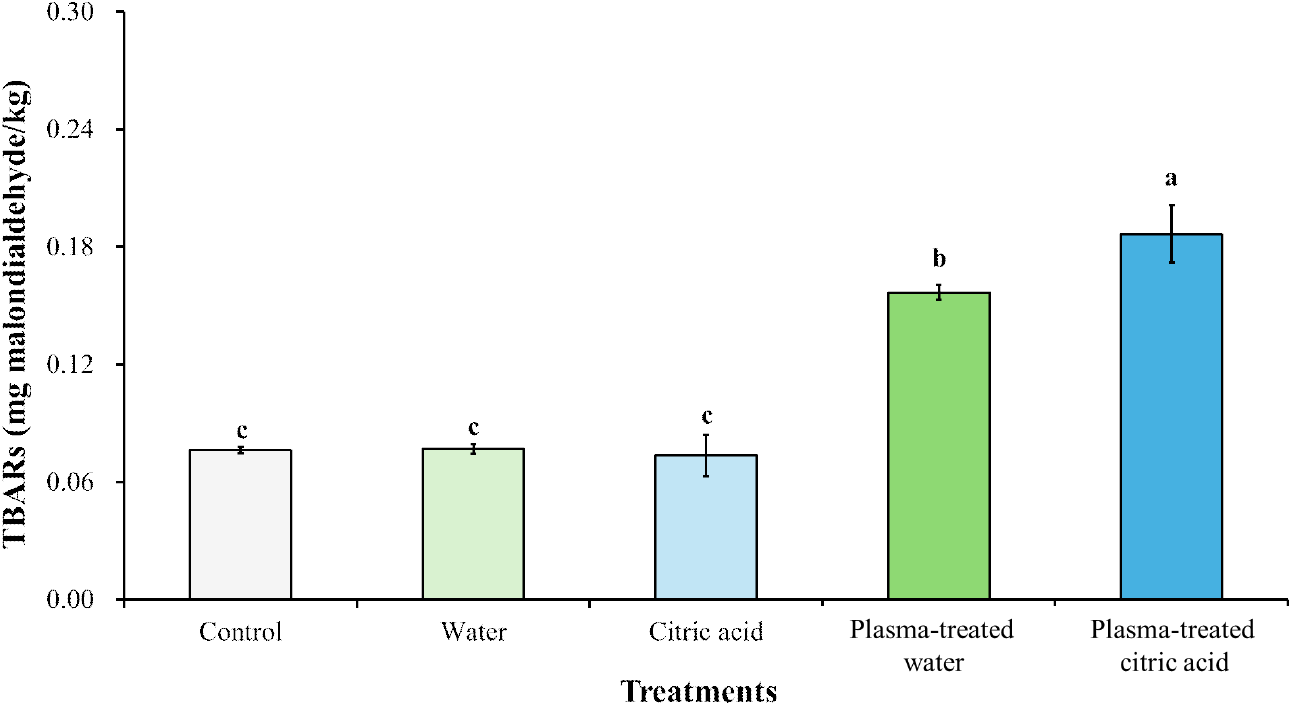
오리고기를 포함한 육류 제품 내 지방산화는 영양 성분의 손실, 산패, 색도 변화를 유발할 수 있으므로, 지방산화가 발생하지 않는 것이 품질로서 중요하다(Yu et al., 2022; Yong et al., 2023). 특히 오리고기는 불포화지방산 함량이 높아 외부 요인에 의한 지방 산화에 취약하며, 다중불포화지방산의 과산화 반응을 통해 MDA와 같은 최종 산화 생성물이 형성될 수 있다(Shin et al., 2019).
본 연구에서 각 세척수로 세척된 오리 껍질의 MDA 함량은 모두 Tarladgis et al.(1960)이 제시한 관능적 산화취 인지한계치인 0.5~1.0 mg MDA/kg 이하로 나타나, 세척으로 인한 이취 발생 가능성은 낮은 것으로 판단된다. 그러나 세척수의 종류에 따라 TBARs 값에는 유의적인 차이가 관찰되었다. Plasma-treated water로 세척된 오리 껍질의 경우 control 대비 유의적으로 높은 MDA 함량을 나타냈는데, 이는 plasma-treated water 내 존재하는 다양한 활성종이 세척 과정 중 오리 껍질의 지질 성분과 직접적으로 반응하여 지방 산화를 유도했기 때문으로 사료된다. 이러한 결과는 플라즈마 처리 과정에서 생성된 활성종이 육류 내 지질과 반응하여 과산화물 및 지방 산화 반응을 유발하고, 이에 따라 TBARs 값이 증가할 수 있다고 보고한 선행 연구들과도 일치하는 경향을 보인다(Wang et al., 2021; Jyung et al., 2023; Lee et al., 2023b). 한편, plasma-treated citric acid로 세척된 오리 껍질은 본 실험에서 가장 높은 TBARs 값을 나타냈다(Fig. 4). 이는 유기산과 플라즈마의 복합 처리 과정에서 오리 껍질 내 지질이 유기산에 의한 pH 감소와 플라즈마 처리로 생성된 활성종의 복합적인 작용에 의해 더욱 촉진된 산화 반응을 겪었음을 시사한다. 선행 연구에 따르면, 유기산에 의한 pH 감소는 플라즈마 처리 과정에서 생성된 활성종의 유기물과의 반응성을 증가시켜 지방 산화를 촉진할 수 있는 것으로 보고되었다(Jyung et al., 2023). 또한 Lee et al.(2023b)은 유기산에 플라즈마 처리를 적용했을 때, 처리 직후 닭가슴살에서 유기산 단독 처리보다 더 높은 수준의 지방 산화가 관찰되었다고 보고하였으며, 이는 본 연구 결과와 동일한 경향을 나타낸다.
그러나 앞서 언급한 바와 같이, 본 연구에서 세척된 모든 오리 껍질의 TBARs 값은 관능적으로 산화취가 인지되는 수준 이하로 나타났으며, 이에 따라 세척으로 인한 이취 발생 가능성은 제한적인 것으로 판단된다. 다만, 이와 같은 수준의 지방 산화 또한 오리 껍질의 색에 변화를 나타낼 수 있으므로, 세척에 따른 오리 껍질의 색 변화를 추가적으로 분석하였다.
Table 2는 각 세척수에 따른 오리 껍질의 색도 변화를 L*, a* 및 b* 값으로 나타낸 것이다. 각 세척수 세척 후 오리 껍질의 L* 값과 b* 값은 control과 비교하였을 때 유의적인 차이를 보이지 않았다(P>0.05). 반면, a* 값의 경우 control과 비교하여 water로 세척된 오리 껍질에서는 유의적인 변화가 관찰되지 않았으나, citric acid, plasma-treated water 및 plasma-treated citric acid로 세척된 오리 껍질에서는 유의적으로 감소하였다(P<0.05). 특히 citric acid로 세척된 오리 껍질의 a* 값은 plasma-treated water 및 plasma-treated citric acid로 세척된 오리 껍질과 비교하여 유의적으로 높은 값을 나타냈으며(P<0.05), plasma-treated water와 plasma-treated citric acid로 세척된 오리 껍질 간에는 a* 값에서 유의적인 차이가 관찰되지 않았다(P>0.05). 이러한 결과는 plasma-treated water이 citric acid보다 오리 껍질의 적색도를 더 크게 감소시켰음을 시사하며, citric acid와 플라즈마를 병행한 plasma-treated citric acid 세척에 따른 추가적인 적색도 감소 효과는 제한적인 것으로 판단된다.
이와 같은 a* 값의 감소는 세척 과정 중 오리 껍질에 존재하는 미오글로빈(myoglobin)의 변성에 기인한 것으로 판단된다. Jeon et al.(2024)는 식육의 pH 감소는 미오글로빈의 변성과 함께 근원섬유 내 공간에 변화를 주어 식육 색도에 영향을 줄 수 있다고 보고하였다. Renerre et al.(1990)은 pH 5.0 아래의 조건에서 미오글로빈 내에 존재하는 포르피린 고리(porphyrin ring)가 변성될 수 있으며, 이때 녹색 색소가 생성될 수 있다고 보고하였다. Ham(2025)는 미오글로빈의 산화가 식육의 a* 값 감소에 중요한 요인으로 작용할 수 있음을 제시하였다. 또한 Kim et al.(2013)은 식육이 H2O2 및 산소와 반응하면 미오글로빈이 choleglobin으로 변환되며 육류의 적색도를 감소시켜 a* 값의 저하를 초래할 수 있다고 보고하였다. Yong et al.(2019)은 플라즈마에 의해 생성된 NO2−는 미오글로빈을 nitrimyoglobin으로 전환시켜 식육의 a* 값을 감소시킬 수 있다고 보고하였다. 이러한 이유들로 본 연구에서 세척된 오리 껍질의 a* 값의 감소가 발생한 것으로 사료된다.
한편, 오리 껍질은 근육 부위에 비해 미오글로빈 함량이 낮고 지방 및 결합조직의 비율이 높은 조직 특성을 가지므로, 본 연구에서 관찰된 적색도 변화는 육색 전반의 변화보다는 표면 색상의 미세한 변화에 해당한다. 따라서 이러한 색도 변화가 소비자 인식 또는 기호도에 미치는 영향은 제한적일 가능성이 있으나, 이에 대한 정량적 평가는 추가적인 소비자 관능 평가를 통해 확인될 필요가 있다.
결론적으로, plasma-treated citric acid는 세척 과정에서 오리 껍질에 존재하는 E. coli O157:H7과 S. enteritidis를 효과적으로 불활성화할 수 있는 세척용액으로 평가되었다. 다만, 세척 처리에 따라 나타나는 오리 껍질의 품질 변화는 소비자의 인식 및 기호도에 영향을 줄 수 있으므로, 향후 소비자 관능 평가를 포함한 추가 연구가 필요할 것으로 판단된다.
적 요
본 연구는 오리 도축 공정의 세척 단계에 적용 가능한 세척수의 활용 가능성을 평가하기 위하여, 오리 껍질 시료를 이용해 서로 다른 세척수(water, citric acid, plasma-treated water, 그리고 plasma-treated citric acid)의 E. coli O157:H7 및 S. enteritidis의 불활성화 효과 및 품질 변화를 비교 분석하였다.
그 결과, citric acid 또는 plasma-treated water 단독 세척에 비해 plasma-treated citric acid가 오리 껍질 내 두 분변성 미생물에 대해 가장 우수한 미생물 불활성화 효과를 나타냈다. 또한 plasma-treated citric acid로 세척한 오리 껍질은 세척 후 control과 비교하여 TBARs 값의 증가 및 a* 값의 감소가 관찰되었으나, L* 및 b* 값에는 유의적인 변화가 나타나지 않았으며, TBARs 값은 관능적으로 이취가 인지되는 수준 이하로 나타났다. 이러한 결과는 plasma-treated citric acid 세척이 두 분변성 미생물에 대해 효과적인 미생물 불활성화 효과를 나타내면서 오리 껍질의 전반적인 품질 저하를 최소화할 수 있음을 시사한다.
다만, 본 연구는 실제 도축 공정을 완전히 모사하지 못한 한계를 지니므로, 향후 추가적인 검증을 통해 산업적 적용 가능성을 확인할 필요가 있다. 그럼에도 불구하고, 본 연구는 water, citric acid, plasma-treated water 그리고 plasma-treated citric acid의 미생물 저감 효과를 비교함으로써, 오리 도축 세척 공정에 적용 가능한 세척수 조합의 가능성을 제시했다는 점에서 의의를 가진다. 특히 plasma-treated citric acid가 citric acid 또는 plasma-treated water 단독 세척보다 향상된 살균 효과를 나타낸다는 점을 확인하였으며, 이는 구연산에 의한 산성 환경과 플라즈마 유래 반응성 화학종의 복합적인 작용에 기인한 결과로 판단된다. 이러한 결과는 plasma-treated citric acid를 도축 공정의 세척수로 활용하기 위한 과학적 근거를 제공하며, 향후 실제 도체를 이용한 세척 조건의 최적화 및 산업적 적용 가능성 평가를 위한 기초 자료로 활용될 수 있을 것이다.

