서 론
전 세계적으로 1인당 소득 증가에 따라 동물성 식품의 소비가 지속적으로 증가하고 있으며, 그중 닭고기는 전체 육류 생산량의 약 29% 이상을 차지할 정도로 높은 비중을 보이고 있다(Oh et al., 2022; Chang and Han, 2025). 닭고기 산업은 다른 축산 분야에 비해 낮은 생산 비용, 생산 기술의 효율적 활용, 변화하는 영양 소비 트렌드와의 부합성, 그리고 빠른 자본 회전율 등의 경쟁력을 바탕으로 전 세계적으로 지속적인 성장세를 보이고 있다(Kim et al., 2025; Pîrlea et al., 2025). 그러나 닭고기를 포함한 동물성 식품 생산 과정에서는 혈액, 뼈, 고기, 지방, 발, 내장 및 피부와 같은 다양한 부산물이 다량 발생한다(Mehmood et al., 2024). 이에 따라 최근에는 자원의 효율적 활용과 환경적 지속가능성을 고려하여 혁신적인 기술과 산업적 접근을 통한 축산 부산물의 활용이 전 세계적으로 장려되고 있다(Lin et al., 2025). 다양한 부산물 중 닭 간은 일반적으로 닭 도체 중량의 약 2.5%를 차지하며, 도축 과정에서 매년 약 2.56만 톤의 부산물이 발생하는 것으로 보고되고 있다(Wang et al., 2025). 이러한 닭 간은 단백질, 지방 및 탄수화물과 같은 주요 영양소뿐만 아니라 칼슘, 인, 철 등의 미네랄과 비타민 A, B1, B2 및 C 등의 비타민을 풍부하게 함유하고 있어 영양학적 가치가 높은 식품 자원으로 평가된다(Zou et al., 2023).
닭 간은 전 세계적으로 다양한 전통 동물성 식품 요리에서 다른 재료와 함께 튀김 또는 반죽 형태로 조리되어 소비되고 있으며(Qu et al., 2021), 이와 같은 식품 용도뿐만 아니라 동물 사료의 원료로도 널리 활용되고 있다(Ibarz-Blanch et al., 2023). 특히 최근에는 반려동물 산업의 성장과 함께 닭 간 분말 및 동결건조 닭 간과 같은 가공 제품 형태로 제조되어 반려동물 간식 등의 원료로도 이용되고 있다(Gwak and Kim, 2025).
그러나 이러한 닭 간을 포함한 닭 부산물은 생산 및 도축 과정에서 미생물에 의해 쉽게 오염될 수 있으며, 특히 도축 과정에서 발생하는 미생물 교차 오염은 완전히 방지하기 어려워 부패 미생물의 존재가 공급업체, 소비자 및 공공 보건 측면에서 중요한 문제로 인식되고 있다(Dourou et al., 2021; Song et al., 2021). 또한 소비자가 구매하는 닭 간의 미생물학적 품질은 도축, 가공 및 포장 단계에서의 위생 관리뿐만 아니라 유통 및 운송 과정에서의 취급 조건(저장 온도, 저장 기간 및 위생 상태 등)이 영향을 주는 것으로 보고되고 있다(Dourou et al., 2021). 일반적으로 가금육은 미생물 증식으로 인해 저장 안정성이 제한적이며, 냉장 조건에서도 도계 후 약 7일 이내에 부패가 진행되는 것으로 알려져 있다(Kim et al., 2021). 따라서 초기 미생물 오염 수준과 저장 및 유통 조건에 따라 부패 진행 속도가 크게 달라질 수 있으므로 실제 유통 및 소비 단계에서 닭 부산물의 위생적 관리와 품질 유지가 매우 중요하다. 특히 우리나라의 경우 여름과 겨울 사이의 기후 편차가 크게 나타나기 때문에 유통 및 소비 과정에서 미생물 증식에 따른 식품 품질 변화가 발생할 가능성이 높다(Kim et al., 2021; Park et al., 2024).
이러한 문제를 해결하고 식품의 안전성을 확보하기 위해 생산 및 가공 환경 조건에서 미생물의 성장, 생존 및 사멸을 수학적으로 분석하고 예측하는 미생물 예측 모델(predictive microbiology)에 대한 연구가 활발히 이루어지고 있다(Tarlak, 2023). 미생물 예측 모델은 식품이 위생적으로 생산 및 유통될 수 있도록 관리 방안을 마련하기 위해, 식품 내 존재하는 미생물의 성장 및 사멸 과정을 특정 매개변수들을 활용한 수학적 모델을 통해 정량적으로 분석하고 예측하는 연구이다(Cho et al., 2024). 미생물 예측 모델은 pH, water activity(Aw), sodium chloride(NaCl) 함량과 같은 내부 요인과 온도, 시간 및 대기 상태 등의 외부 요인을 반영하여 식품 중 미생물의 성장 및 정량적 변화를 예측할 수 있는 중요한 도구로 활용되고 있다(Meinert et al., 2023). 기존 연구에서는 미생물 예측 모델을 활용하여 닭 다리, 닭 날개, 닭 가슴살 등 다양한 닭고기 제품에서 저장 온도에 따른 미생물 성장 패턴을 예측하고, 이를 바탕으로 제품의 유통기한을 설정하기 위한 연구가 보고된 바 있다(Tashiguano, 2025). 하지만 다양한 온도 조건에서 저장된 닭 간에서 미생물 예측 모델을 개발한 연구는 매우 부족한 실정이다.
예측 모델 개발에는 주로 Baranyi model과 Gompertz model이 널리 사용되는데, 두 model 모두 온도가 증가하면 유도기 시간(lag phase duration)은 감소하고 최대 성장률(maximum growth rate)은 증가하는 많은 연구가 보고되어왔다(Tarlak, 2023; Cho et al., 2024; Juneja et al., 2025). 일반적으로 Baranyi model은 미생물이 새로운 환경에 적응하는 유도기에서 초기 생리적 상태를 묘사하는 데 강점이 있는 것으로 알려져 있다(Baranyi and Roberts, 1994). 반면, Gompertz model은 비대칭적인 시그모이드 곡선을 피팅하는 데 있어 통계적 유연성이 높아 복잡한 성장을 안정적으로 묘사하는 특징이 있다(Zwietering et al., 1990). 이에 본 연구에서는 닭 간의 생산 과정에서 저장, 운송 중에 성장할 수 있는 미생물에 대해 닭 간의 미생물학적 수준을 확인하기 위하여 다양한 온도 조건(4, 15, 25 및 30°C)에서 저장 기간에 따른 총 호기성 미생물의 수를 측정하였다. 이후 Baranyi model과 Gompertz model을 적용하여 닭 간에서 총 호기성 미생물 성장의 예측 모델을 개발하고 두 예측 모델의 성능을 평가함으로써, 닭 간에서 총 호기성 미생물의 성장을 설명하는 최적의 모델을 선정하고 이를 기반으로 정량적 예측 모델을 개발하고자 한다.
재료 및 방법
닭 간 시료는 대전광역시 중구에 위치한 전통시장의 닭 부산물 소매점에서 도축 후 48시간 이내의 생 닭 간을 구입하였으며, 구매 당일 실험에 사용하였다. 실험의 객관성을 확보하기 위해 동일 배치의 서로 다른 개체에서 채취한 시료를 사용하였으며, 모든 실험은 2회 반복 수행하여 평균값을 산출하였다. 닭 간은 표면의 핏물을 제거한 후 무균 작업대에서 20 g씩 소분하고 함기 포장(polyethylene bags, 20 × 30 cm) 하였으며, 4, 15, 25 및 30°C의 저장 온도 조건에서 각각 10, 8, 6 그리고 6일간 저장하였다. 본 연구의 저장 온도는 닭 간이 실제 유통, 저장 및 소비 과정에서 노출될 수 있는 다양한 온도 조건을 반영하기 위함이다. 4°C는 냉장 보관 온도를, 15°C는 유통 과정 중 일시적인 온도 이탈 상황을 가정하였다. 또한, 25°C와 30°C는 하절기 상온 노출이나 소비 중 발생할 수 있는 상온 방치 상태를 가정하여 설정하였다.
다양한 저장 온도 조건에서 닭 간의 총 호기성 미생물은 식품공전의 일반 미생물 실험 법을 기반으로 실험하였다. 멸균 샘플 백(3M, USA)에 시료 20 g과 0.85% 멸균 생리식염수 180 mL를 넣고 stomacher(BagMixer® 400, Interscience, France)를 이용하여 1분 동안 균질화하여 10배 희석하였다. 균질화된 시료는 0.85% 멸균 생리식염수를 이용하여 십진 희석을 진행하였으며, 희석된 시료 0.1 mL를 plate count agar(PCA, MB cell, Korea)에 도말하여 총 호기성 미생물 수를 확인하였다. 배지는 37°C에서 24시간 동안 배양하였으며, 배양 후 배지 위에 형성된 균체(colony)를 계수하여 log colony forming unit(CFU)/g으로 측정하였다.
닭 간에서 총 호기성 미생물의 성장을 표현하기 위해 Baranyi and Roberts(1994)가 제시한 Baranyi function을 사용하였다. 총 호기성 미생물의 저장 온도에 따른 정량적 분석을 기준으로 Baranyi function에 대입하여 수학적 모델을 도출하였다. DMFit(3.5 version)을 사용하여 수학적 모델의 매개변수인 초기 미생물 수(initial microbial count, y0), 최대 미생물 수(maximum microbial count, ymax), 최대 성장률(maximum growth rate, μmax)과 유도기 시간(lag phase duration, LPD)을 구하였다. Baranyi model 수식은 아래와 같다.
N(t) : 시간 t에서의 미생물 값(log CFU/g)
y0 : 초기 미생물의 값(log CFU/g)
ymax : 최대 미생물 값(log CFU/g)
μmax : 최대 성장률(log CFU/g/h)
t : 시간(h)
위 수식에서 h0값은 미생물의 초기 생리적 상태, 즉 미생물이 환경에 적응하는 정도를 나타내는 매개변수로, μmax와 LPD의 곱으로도 나타낼 수 있다. A(t)는 시간에 따른 보정 인자로 lag phase에서 exponential phase로 전환을 매끄럽게 해 주는 매개변수이다. 모든 결과는 log CFU/g로 표시하였다.
닭 간에서 총 호기성 미생물의 성장을 표현하기 위해 Gompertz(1825)가 제시한 Gompertz model을 사용하였다. Gompertz model은 미생물 생장 곡선의 유도기, 대수기, 정지기를 포함하는 전형적인 시그모이드 곡선을 정확하게 표현하는 비선형 모델이다. 본 연구에서는 저장 온도에 따른 총 호기성 미생물 수의 정량적 분석을 기준으로 Gompertz model 수식에 대입하여 매개변수 값을 도출하였다. 그리고 도출된 매개변수를 통해 SigmaPlot(10.0 version)을 사용하여 초기 미생물 수(initial microbial count, y0), 최대 미생물 수(maximum microbial count, ymax), 최대 성장률(maximum growth rate, μmax)과 유도기 시간(lag phase duration, LPD)을 계산하였다. Gompertz model의 수식은 다음과 같다.
N(t) : 시간 t에서의 미생물 값(log CFU/g)
y0 : 초기 미생물 값(log CFU/g)
a : 최대 미생물 값에서 초기 미생물 값을 뺀 값(log CFU/g)
x0 : 미생물 성장률이 최대인 시간, 변곡점 지점
b : 미생물 성장률에 관여하는 매개변수
t : 시간(h)
위 수식을 통해 ymax, 최대 미생물 값(log CFU/g)은 y0과 a의 합으로 계산하였고 μmax는 으로 계산하였으며 LPD는 x0−b로 계산하였다(Costa, 2008). 모든 결과는 log CFU/g로 표시하였다.
닭 간에서 온도에 따른 최대 성장률과 유도기 시간의 변화를 표현하기 위해 Excel spreadsheet(Microsoft Office 365)에서 1차 모델 매개변수를 이용하여 2차 모델을 개발하였다.
Baranyi model과 Gompertz model로 얻은 미생물 성장 예측 모델의 성능과 적합성을 평가하기 위해 R2, 평균 제곱근 오차(root mean square error, RMSE), bias factors(Bf), accuracy factors(Af) 값들을 비교하였다. 각 값은 다음과 같은 식을 통해 계산된다.
위 수식에서 obs는 관측값, pred는 예측값, n은 관측값의 개수, 는 관측값의 평균을 나타낸다. R2은 회귀분석에서 모델이 종속변수의 분산을 독립변수로 얼마나 잘 설명하는지를 나타내는 지표이다. R2은 0에서 1사이의 값을 가지며, 1에 가까울수록 모델이 데이터에 적합하고, 0에 가까울수록 적합도가 낮다고 해석할 수 있다. RMSE는 수학적 모델의 성능을 평가할 때 이용하며 모델의 예측값과 관측값 사이의 오차 크기를 측정한다. Bias factors는 예측값과 실제로 관측한 값의 상대적 편차의 측정이며, Accuracy factors는 예측치가 얼마만큼 관측치와 차이 나는지를 측정한 값을 의미한다.
1차 모델 매개변수를 활용하여 개발된 2차 모델 예측의 적합성을 평가하고 개발된 예측 모델의 예측 성능을 평가하기 위하여 허용 가능한 예측 영역(acceptable prediction zone, APZ) 분석을 진행하였다. APZ 분석은 예측 모델의 예측 오차가 허용 가능한 영역 이내에 존재하는지 판단하는 분석 방법으로, APZ 분석 결과 예측 오차의 70%가 APZ 한계 영역 이내에 존재해야 허용 가능한 예측 모델로 판단한다(Oscar, 2023). APZ 분석의 예측 오차는 각 온도의 관측값에서 예측값을 뺀 값으로 계산되었으며, APZ 한계 영역은 −1.0 log CFU/g에서 0.5 log CFU/g으로 설정되었다(Oscar, 2023). APZ 분석을 위해 1차 모델 피팅에 사용하지 않은 온도(10 및 20°C) 조건에서 추가 실험을 진행하고, 개발된 2차 모델을 통해 예측값을 계산하여 얻은 데이터를 2차 모델 검증에 사용하였다.
결과 및 고찰
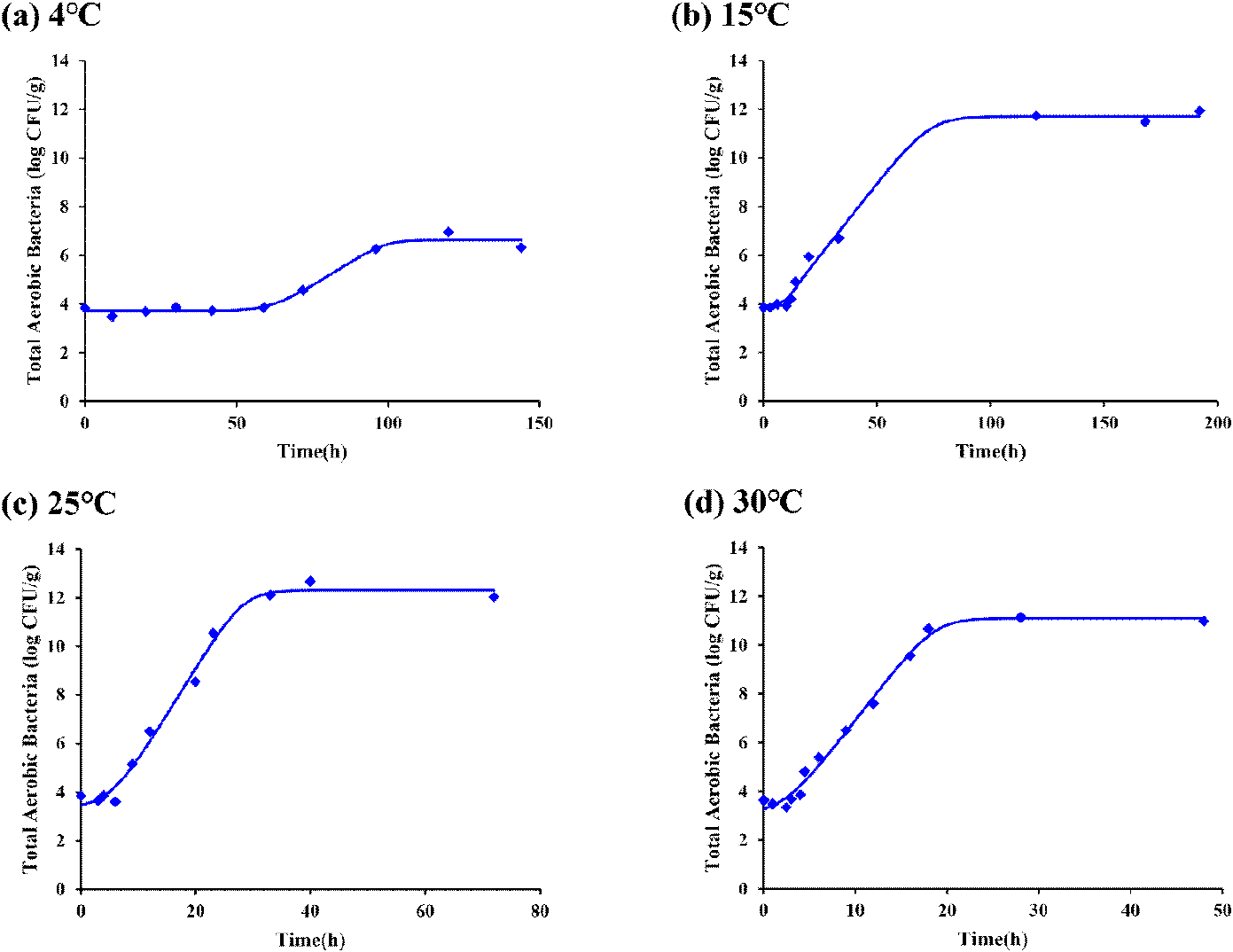
예측 모델을 개발하기 위한 1차 모델의 개발은 중요하며, 미생물의 수를 예측하는 데 있어서 다양한 수학적 모델(Baranyi model, Gompertz model, logistic model 등)이 이용될 수 있다. 따라서 각 수학적 모델을 개발하고 비교, 검증하여 모델의 적합성을 평가할 필요가 있다. 이에 본 연구에서는 Baranyi model과 Gompertz model을 적용하여 온도별 저장 기간에 따른 닭 간에서 총 호기성 미생물 성장 예측 모델을 개발하였다. Figs. 1 and 2는 각각 Baranyi model과 Gompertz model로 개발된 각 온도별 저장 기간에 따른 총 호기성 미생물 성장의 1차 모델을 나타내며, Baranyi model과 Gompertz model로 개발된 1차 모델 모두 모든 온도 조건에서 시그모이드 형태의 미생물 성장 곡선을 보여주었다. 개발된 Baranyi model과 Gompertz model 1차 모델의 각 온도별 매개변수인 초기 미생물 값, 최대 미생물 값, 최대 성장률, 유도기 시간을 계산하여 Table 1에 나타내었다. 그 결과 Baranyi model에서 초기 미생물 값은 3.26 log CFU/g의 미생물 수준으로 시작하였지만 최대 미생물 값은 6.96 log CFU/g에서 12.67 log CFU/g으로 차이가 나는 최대 미생물 값을 얻을 수 있었다. 마찬가지로 Gompertz model에서 초기 미생물 값도 3.30 log CFU/g의 미생물 수준에서 시작하였지만 최대 미생물 값은 6.63 log CFU/g에서 12.52 log CFU/g으로 차이가 나는 최대 미생물 값을 얻을 수 있었다. 그리고 온도 조건에 따른 최대 성장률은 Baranyi model과 Gompertz model에서 각각 4°C에서 0.08과 0.10 log CFU/g/h, 15°C에서 0.12와 0.14 log CFU/g/h, 25°C에서 0.39와 0.44 log CFU/g/h, 그리고 30°C에서 0.49와 0.55 log CFU/g/h로, 저장 온도가 증가함에 따라 최대 성장률이 증가하고 Baranyi model보다 Gompertz model에서 더 큰 경향을 나타냈다. 이에 반해, 유도기 시간은 Baranyi model과 Gompertz model에서 각각 4°C에서 62.01과 64.06 h, 15°C에서 7.23과 7.59 h, 25°C에서 5.34와 6.37 h, 그리고 30°C에서 2.47과 3.20 h로, 저장 온도가 증가함에 따라 유도기 시간이 감소하고 Baranyi model보다 Gompertz model에서 더 긴 경향을 나타냈다.
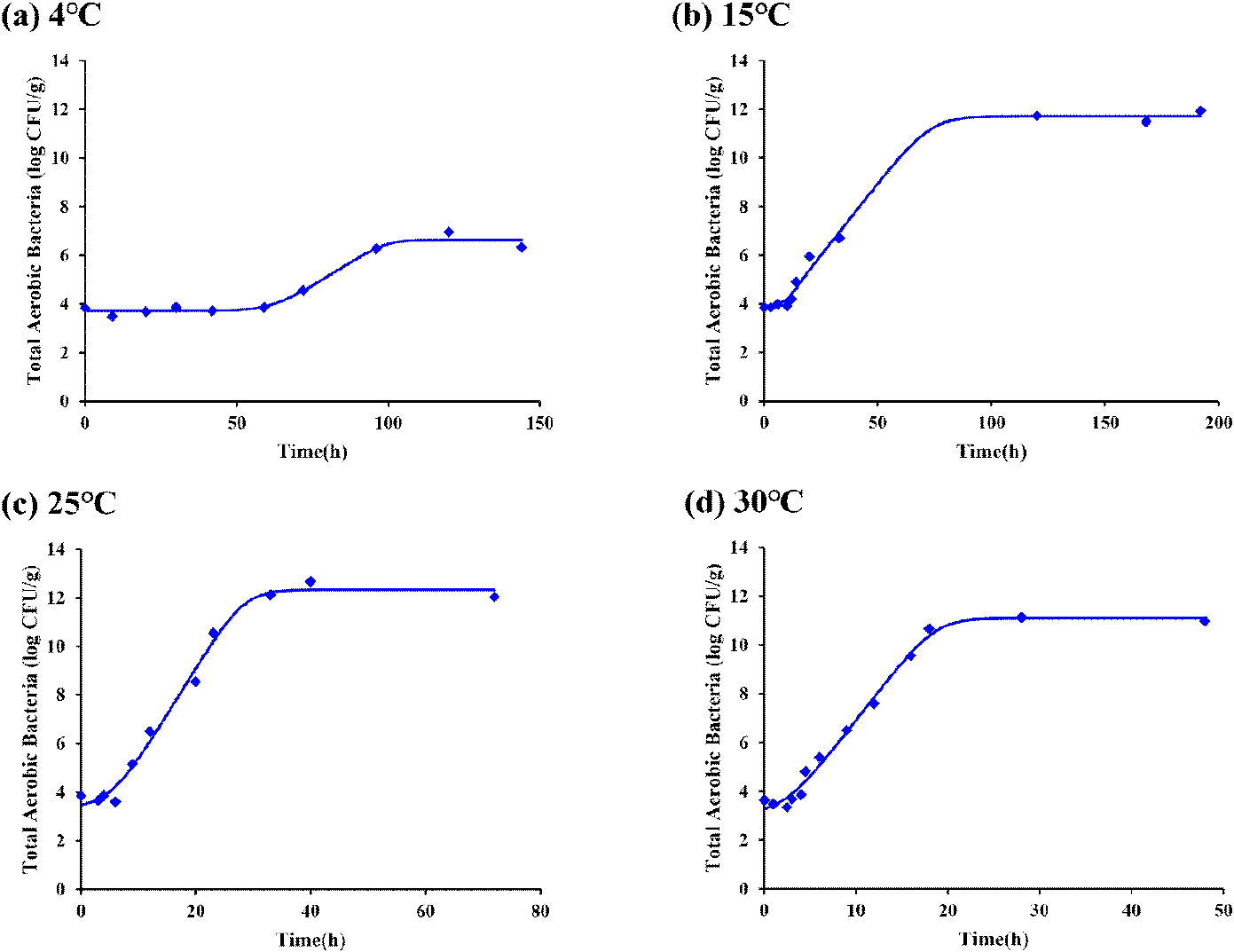
Baranyi model은 생물학적으로 매개변수를 설명하고, 예측 모델의 적용 가능성을 높이는 특징을 가지고 있어 다양한 연구에서 미생물 성장 변화를 파악하는 수단으로 사용한다(Juneja et al., 2025). 또한, Baranyi model은 미생물의 생리학적 적응과 성장에 영향을 주는 요인인 유도기에서 대수기로의 변화를 포착하므로 본 연구에서 1차 모델 개발에 적용하였다. Baranyi and Roberts(1994)의 미생물 성장 기본 모델에 따르면, 초기 미생물 값의 변동은 일반적으로 약 1 log CFU/g 범위 내에서 허용되며, 이는 미생물의 생리적 상태와 성장 시 적응 과정에서 나타나는 자연스러운 변동으로 해석할 수 있다. 이러한 초기 미생물 값의 변동성은 모델 내에서 유도기 시간 및 최대 성장률에 영향을 미치는 주요 변수 중 하나이지만, 동일한 생리적 상태를 가정할 경우 일정한 상수로 처리하여 모델의 안정성을 높일 수 있다고 보고된다. 따라서 본 연구에서 관측된 3.26~3.88 log CFU/g 범위의 초기 미생물 값은 Baranyi model 적용 시 허용 가능한 자연 변동 범위에 해당하며, 미생물 성장 예측 모델 개발에 있어 충분히 유사한 초기 미생물 값으로 간주할 수 있다(Baranyi and Roberts, 1994). 온도 조건에 따른 최대 성장률은 최근 Bacillus cereus 및 총 호기성 미생물에 대해 수행된 연구에서, 동적 온도 변화 환경에서 최대 성장률이 온도의 상승에 비례하여 증가한다고 보고한 바와 일치한다(Martinez-Rios et al., 2025). 따라서 본 연구의 1차 Baranyi model은 기존 선행 연구의 결과와 동등한 경향성을 보이며, 온도 기반 미생물 성장 예측 모델의 타당성을 뒷받침하는 것으로 판단된다(Martinez-Rios et al., 2025). 뿐만 아니라, 저장 온도가 증가함에 따라 유도기 시간이 감소하는 경향은 저장 온도가 미생물의 대사 활성 및 적응 속도를 촉진하여, 높은 온도일수록 유도기가 짧아짐을 의미한다. 본 연구 결과는 온도가 상승하면 유도기 시간이 짧아지는 Tarlak(2023)의 연구 결과와 일치한다.
Gompertz model은 시간에 따른 비선형적 성장을 정교하게 묘사하고, 실험 데이터 군에서 우수한 적합도를 나타내는 특징을 가지고 있어 다양한 연구에서 미생물 성장 변화를 파악하는 수단으로 사용된다(Vaghi et al., 2020). 또한, Gompertz model은 초기 유도기 이후 급격한 증식과 함께 특정 성장률을 포착하여 실제 미생물 증식 데이터와 높은 일치도를 보이므로 본 연구에서 1차 모델 개발에 적용하였다. Gibson et al.(1987)의 연구에 따르면, Gompertz model은 초기 미생물 값의 미세한 변동이 있더라도 데이터의 비선형 회귀분석을 통해 성장 곡선의 특성을 통계적으로 유의미하게 묘사할 수 있다. 따라서 본 연구에서 관찰된 0.44 log CFU/g의 초기 미생물 값의 편차는 일반적인 미생물 계수 오차 범위 내에 있으며, 모델의 신뢰성을 보장하는 데 결함이 되지 않음을 시사한다. 온도 조건에 따른 최대 성장률은 온도가 미생물의 효소 반응 속도 및 대사 효율에 직접적인 영향을 미쳐 세포 분열 속도를 가속화하기 때문이고, 다양한 미생물의 성장 데이터를 Gompertz model로 재매개변수화하여 분석한 결과, 최적 성장 온도 범위 내에서 온도가 상승할수록 최대 성장률이 지수적으로 증가함을 입증하였다(Wang and Guo, 2024). 이러한 결과는 미생물의 운동 에너지가 증가함에 따라 기질 이용 속도가 빨라진다는 일반적인 생물학적 원리와 일치하며, 본 연구에서 Gompertz model로 개발된 1차 모델이 닭 간에서 저장 온도에 따른 총 호기성 미생물의 변화를 적절히 예측하고 있음을 시사한다. 저장 온도가 증가함에 따라 유도기 시간이 감소하는 경향은 고온에서 미생물의 대사 효소 활성이 촉진되어 새로운 환경에 적응하고 세포 분열을 준비하는 데 소요되는 시간이 감소했기 때문이다. Zwietering et al.(1990)은 Gompertz model 매개변수 분석을 통해 온도와 유도기 시간 사이에 강한 음의 상관관계가 있음을 보고하였으며, 이는 본 연구의 결과와 일치한다. 또한, Whiting(1995)은 온도가 최적 생장 온도에 가까워질수록 미생물의 생화학적 반응 속도가 증가하여 결과적으로 유도기가 지수적으로 감소한다는 점을 강조하였다. 이러한 결과는 본 연구에서 Gompertz model로 개발된 1차 모델이 닭 간에서 저장 온도에 따른 총 호기성 미생물의 초기 적응 기작을 생물학적으로 타당하게 반영하고 있음을 뒷받침한다.
적용된 모델을 기초로 직접 관측하지 않은 온도에서 총 호기성 미생물 수를 예측하기 위한 기초 단계로 적절한 1차 모델의 선택은 중요한 단계이다(Fakruddin et al., 2012). 따라서 적합성 평가 지표를 활용하여 닭 간에서 저장 온도에 따른 총 호기성 미생물 성장의 Baranyi model과 Gompertz model로 개발된 1차 모델의 비교 및 검증을 진행하였다. Baranyi model과 Gompertz model의 적합성을 평가하기 위해 결정 계수(R2), 평균 제곱근 오차(RMSE), bias factors(Bf), accuracy factors(Af)를 계산하여 2가지 모델의 적합도 및 통계적 특성을 비교하여 Table 2에 나타냈다. R2은 0과 1 사이의 분수로 모델의 적합도를 정량화하는 데 유용한 지표로 활용되며, R2이 0.9와 1에 위치할수록 특정 모델이 데이터를 잘 설명하고 있다는 것을 의미한다(Asuero et al., 2006). 본 연구에서 개발된 닭 간에서 저장 온도에 따른 총 호기성 미생물 성장 1차 모델은 Baranyi model과 Gompertz model 모두 모든 온도 조건에서 0.90 이상의 R2을 나타냈기 때문에 높은 예측력을 가진다고 판단된다. RMSE는 미생물 예측 모델에서 예측의 오차 정도를 나타내는 지표로, 값이 낮을수록 오차가 작은 것을 의미한다(Baranyi et al., 1999). 본 연구에서 개발한 Baranyi model의 RMSE는 1.664, 0.675, 1.372, 0.836이며, Gompertz model의 RMSE는 0.181, 0.367, 0.398, 0.331으로 확인되었다(Table 2). 개발된 1차 모델의 모든 온도 조건에서 Gompertz model로 개발된 1차 모델의 RMSE가 Baranyi model로 개발된 1차 모델의 RMSE와 비교하여 더 낮게 나타났다. 그러나 RMSE는 절대 오차를 평가하기 때문에 오차가 클수록 RMSE가 커질 수 있지만 이상치에 민감하기 때문에 이로 인해 모델의 성능이 과소평가될 수 있다(Mentaschi et al., 2013). 이에 Ross(1996)는 모델의 검증을 위한 또 다른 지표로 Af와 Bf를 제시했고, Af는 모델의 정확도를 평가하는 지표이며, Bf는 모델이 예측하는 값의 편향을 나타내는 지표라고 설명하고 있다. 이에 추가로 적합성 검증 결과, Baranyi model의 Af는 1.049, 1.008, 1.023, 1.011, Bf는 1.229, 1.107, 1.180, 1.121이었으며, Gompertz model의 Af는 1.005, 1.026, 1.017, 1.021, Bf는 1.001, 0.959, 1.002, 1.002로 확인되었다(Table 2). Ross(1996)의 연구 결과에 따르면 Af는 1에 가까울수록 성능이 더 좋은 모델이며 Bf는 0.9~1.05 범위에 포함될 경우 예측 편향이 적은 좋은 모델로 평가하고 0.7~0.9, 1.05~1.15 범위에 포함될 경우 받아들여질 수 있으며 이외의 값은 받아들여질 수 없다고 평가한다. 이에 따르면 15°C, 30°C의 Af는 Baranyi model의 적합도가 더 우수하고 4°C, 25°C의 Af는 Gompertz model의 적합도가 더 우수하지만, Bf의 경우 모든 온도 조건에서 Gompertz model의 적합도가 우수하게 나타났다. 그뿐만 아니라 Baranyi model로 개발된 1차 모델의 Bf는 4°C, 25°C에서 받아들여질 수 없는 적합도로 계산되었다. 이러한 결과는 Baranyi model이 개별 미생물의 생리적 적응 과정을 반영하는 데 강점이 있는 반면, 본 연구에서 얻은 닭 간의 총 호기성 미생물 성장 데이터는 복합 미생물군의 집합적 성장 양상을 나타내므로, 성장 곡선을 경험적으로 설명하는 Gompertz model이 상대적으로 더 우수한 적합도를 보인 것으로 해석될 수 있다(Winsor, 1932; Baranyi and Roberts, 1994).
결과적으로, 두 가지 유형의 1차 모델 중 Gompertz model로 개발된 1차 모델의 적합도가 Baranyi model보다 전반적인 예측 편향과 정확성 부분에서 우수하게 나타났다. 이는 Gompertz model이 닭 간에서 저장 온도에 따른 총 호기성 미생물의 성장 예측에 더 정확하다는 것을 의미한다.
앞선 1차 모델 비교 분석을 통해 Gompertz model이 Baranyi model보다 높은 통계적 적합성을 보임에 따라, 본 연구에서는 Gompertz model로 개발된 총 호기성 미생물 성장 매개변수를 기반으로 최대 성장률, 유도기 시간 2차 모델을 개발하였다. 개발된 μmax와 LPD의 각 2차 모델의 Excel 수식은 아래와 같다.
μmax(x)=0.0669e0.0695x
LPD(x)=70.639e−0.106x
μmax(x) : 온도 x에서 최대 성장률(log CFU/g/h)
LPD(x) : 온도 x에서 유도기 시간(h)
x : 온도(°C)
Figs. 3A and 3B는 각각 본 연구에서 개발된 닭 간에서 온도에 따른 총 호기성 미생물의 최대 성장률, 유도기 시간의 2차 모델을 나타내며 앞서 말한 것과 같이 1차 모델 매개변수의 경향성과 일치하였다. 최대 성장률에 대한 2차 모델 분석 결과, 온도가 증가함에 따라 최대 성장률은 증가하는 경향을 보였으며, 그래프는 전반적으로 우상향하는 지수함수적 형태를 나타냈다(Fig. 3A). 이는 미생물 성장률과 온도의 관계를 설명하는 Dey et al.(2020)의 연구 결과와 일치한다. Dey et al.(2020)의 연구에서는 온도 증가에 따라 미생물의 최대 성장률이 지수함수적으로 증가함을 보고하였으며, 이와 동일하게 본 연구에서도 온도 증가에 따라 μmax가 비선형적이고 지수적으로 증가하는 패턴이 관찰되었다. 이러한 결과는 총 호기성 미생물의 온도 의존적 성장 특성을 정확히 반영하는 것으로, 예측 모델의 신뢰성을 높이며 저장 온도 변화에 따른 미생물 성장 예측에 효과적으로 활용될 수 있음을 시사한다.
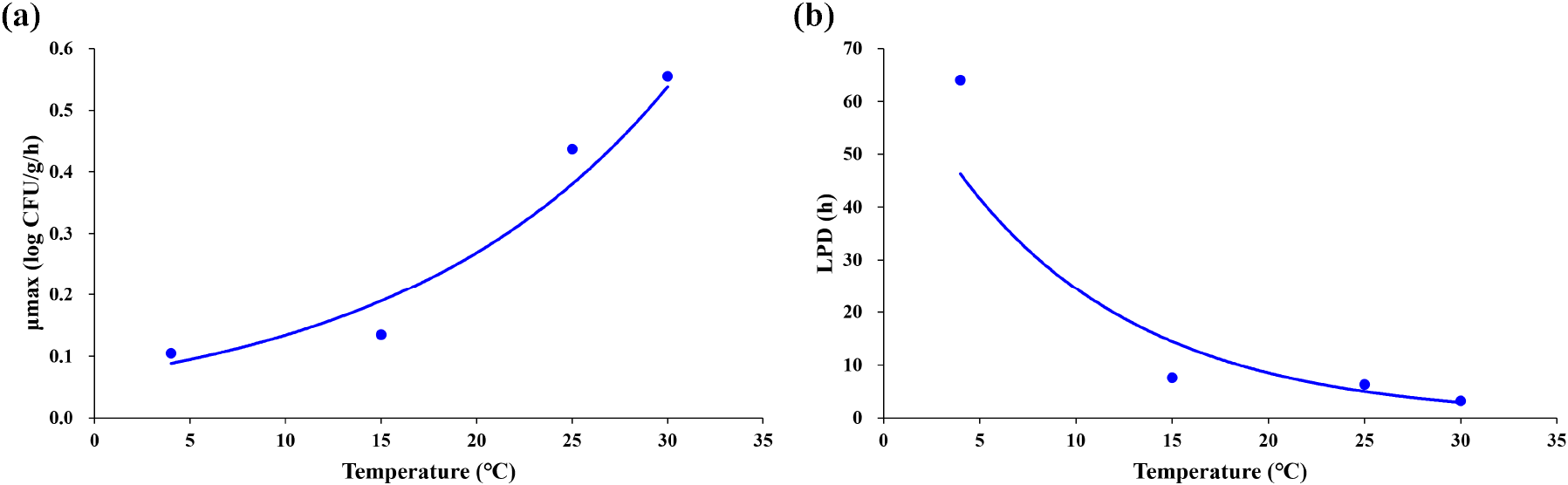
유도기 시간의 2차 모델은 온도가 증가하면 우하향하는 로그 함수 형태의 모델로 개발되었다(Fig. 3B). 이는 앞서 말한 것과 같이 온도 증가가 미생물의 세포 적응 및 대사 활성을 촉진하여 유도기 시간을 단축시키는 현상을 반영한 결과로 판단된다(Dey et al., 2020). 본 연구에서 확인된 유도기 시간의 로그함수적 감소 경향은 Garre et al.(2025)이 제시한 2차 모델 결과와 유사하였다. 해당 연구에서도 온도 상승에 따라 유도기 시간이 로그함수적으로 감소하는 것으로 나타났다. 따라서 본 연구의 유도기 시간 모델은 최신 연구 동향과 부합하며, 미생물 성장 예측의 정확도와 현실 반영 측면에서 유의미한 의의를 가진다.
본 연구에서 개발된 모델의 예측력과 예측 모델의 성능의 적합성을 평가하기 위해 1차 모델과 2차 모델 개발에 사용되지 않은 온도 조건인 10 및 20°C 조건에서 2차 모델을 이용하여 검증을 실시하였다. 그리고 1차 모델 개발과 같은 방식으로 온도 조건에 따른 총 호기성 미생물의 정량적 분석 실험을 진행하였다. 그 후, 예측 모델의 매개변수와 관측값의 매개변수를 비교하여 적합성 평가 계수를 계산하여 검증을 진행하였다. 계산된 적합도는 Table 3에 나타냈다. R2는 모든 온도 조건에서 0.99로 높은 예측력을 가진 예측 모델이라는 결과를 얻을 수 있었다. 본 연구에서 개발한 예측 모델의 RMSE는 검증 온도(10 및 20°C)에서 각각 0.169, 0.358의 값을 나타내어 우수한 예측력을 보였다. 뿐만 아니라, 10°C와 20°C 조건에서 Af가 각각 1.005, 1.016, Bf가 각각 1.001, 0.991으로 나타났다. Baranyi et al.(1999)은 RMSE가 예측 미생물 모델의 오차 정도를 정량적으로 평가하는 데 유용한 지표임을 제시하고 있으며, 본 연구에서도 RMSE의 결과가 낮아 예측 모델의 신뢰성을 입증하였다. Mohammad et al.(2025)의 연구 결과와 같이 RMSE가 낮은 것뿐만 아니라 1 이하일 경우 우수한 예측력과 모델 성능을 나타낸다고 제시하고 있다. 본 연구 결과는 기존 연구의 기준과 일치하며, 닭 간에서 온도 기반 총 호기성 미생물의 성장 예측에 있어 모델의 신뢰성과 실용성을 입증한다고 평가할 수 있다. 본 연구의 Af, Bf 결과는 모두 Ross(1996)의 기준을 만족하므로, 모델의 적합성이 뛰어난 것으로 판단된다. 이러한 결과로 닭 간에서 온도 기반 총 호기성 미생물의 성장 모델 검증 지표로서 Af 및 Bf의 활용은 개발된 예측 모델의 실용성과 신뢰성을 뒷받침한다. 이러한 적합도 평가 결과를 바탕으로 본 연구의 모델은 저장 온도에 따른 총 호기성 미생물의 성장 예측에 적용하기에 적합함을 확인할 수 있다.
| Temperature (°C) | R21 | RMSE2 | Af3 | Bf4 |
|---|---|---|---|---|
| 10 | 0.99 | 0.169 | 1.005 | 1.001 |
| 20 | 0.99 | 0.358 | 1.016 | 0.991 |
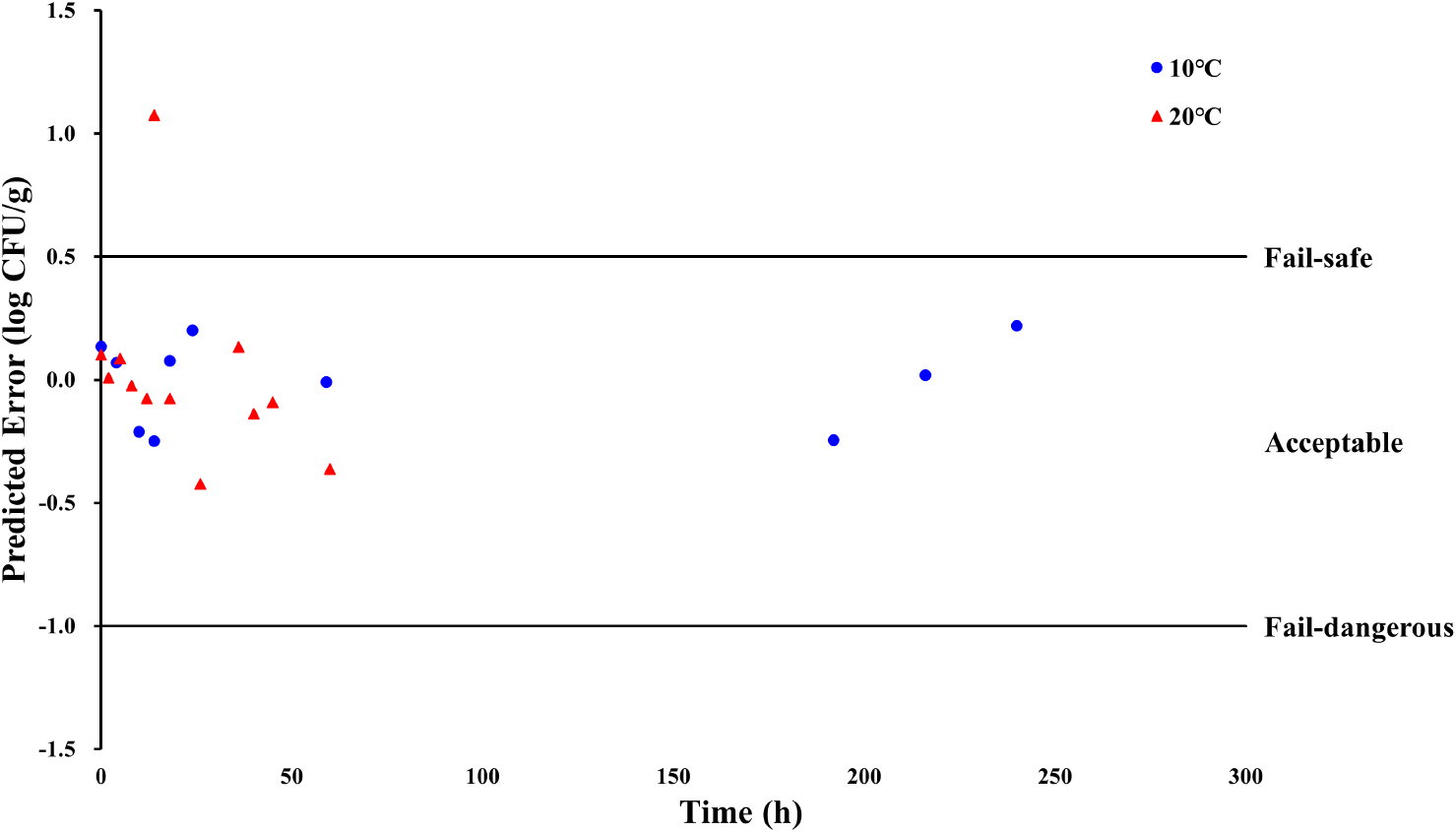
10 및 20°C 조건에서 개발된 예측 모델의 적합성을 검증하기 위해 관측값과 모델 예측값 간의 차이를 계산하여 예측 오차를 도출하였으며, 해당 오차값을 이용하여 acceptable prediction zone(APZ) 분석을 실시하였다. Fig. 4는 APZ 분석 결과로 10°C 예측 모델의 예측 오차 10개 중 10개와 20°C 예측 모델의 예측 오차 12개 중 11개가 APZ 한계 영역 이내에 존재하여 최종 95.45%의 예측 오차 값이 APZ 한계 범위 내에 속하였다. Juneja et al.(2025)의 연구에 따르면 전체 예측 오차 중 70% 이상이 APZ 허용 범위 내에 들어오면 허용 가능한 성능으로 간주할 수 있다. 따라서 이는 2차 모델의 수행이 허용 가능하다는 것을 나타낸다. 안전 한계를 벗어나는 예측 오차는 모델의 과대 예측을 의미하며, 이는 실제로는 안전할 수 있는 식품을 불필요하게 폐기하게 만드는 결과를 초래할 수 있다. 반면, 위험 한계를 벗어나는 예측 오차는 모델의 과소 예측을 의미하며, 이는 안전하지 않은 식품의 소비로 이어져 식중독 발생 위험을 증가시킬 수 있다(Juneja et al., 2025). 이에 본 연구에서 개발된 예측 모델은 95.45%의 예측 오차 값이 APZ 한계 범위 내에 속하였으므로 높은 예측 수행 능력을 가진 예측 모델 개발된 것으로 확인된다.
적 요
본 연구에서는 닭 간의 생산 이후 저장 및 운송 과정에서 증식할 수 있는 총 호기성 미생물을 분석함으로써 닭 간의 미생물학적 안전성을 평가하고자 하였다. 이를 위하여 4, 15, 25 및 30°C의 다양한 온도 조건에서 저장 기간에 따른 총 호기성 미생물 수를 측정하여 온도에 따른 미생물 증식 특성을 분석하였다. 이후 Baranyi model과 Gompertz model을 적용하여 미생물 예측 모델을 비교하여 개발하고 검증하였다. 개발된 다양한 온도 조건에서 저장된 닭 간의 총 호기성 미생물 1차 모델은 시그모이드 형태의 성장곡선을 나타냈으며 모든 1차 모델 매개변수가 초기 미생물 값은 3.26 log CFU/g에서 3.88 log CFU/g으로 유사한 미생물 수준으로 시작하였지만, 온도가 증가하면 최대 성장률은 증가하고 유도기 시간은 짧아지는 것을 확인할 수 있었다. 또한, Baranyi model, Gompertz model 1차 모델을 검증한 결과 Gompertz model의 검증값이 Baranyi model의 검증값보다 우수한 수치를 나타내었다. 이에 Gompertz model의 매개변수를 기초로 하여 Excel spreadsheet로 2차 모델을 개발하였다. 1차 모델과 2차 모델로 개발된 예측 모델은 통계적 적합성과 외부 검증을 통해 높은 신뢰성을 입증하였다. 이에 본 연구에서 개발된 닭 간에서 총 호기성 미생물 성장의 온도 기반 예측 모델은 미생물학적 수준을 평가하고 저장 기간을 예측할 수 있을 것이며, 예측 모델을 통한 다양한 온도의 최대 성장률 및 유도기 시간의 예측력을 확보하여 경제적 비용을 절감하고 식품 폐기물을 감소시킬 수 있을 것으로 판단된다.
그러나 본 연구에서는 등온 조건에서의 예측 모델만을 개발하였기 때문에, 실제 유통 및 소비 과정에서 발생할 수 있는 비등온(동적) 온도 변화에 따른 미생물 증식을 정밀하게 예측하는 데에는 한계가 있다. 따라서 향후 연구에서는 닭 간 내 총 호기성 미생물의 동적 온도 조건을 반영한 예측 모델을 개발하고, 이를 실험적으로 검증할 필요가 있다. 아울러, 개발된 모델의 현장 적용성을 확보하기 위하여 실시간 온도 모니터링과 연계된 품질 관리 시스템 구축에 관한 추가 연구가 요구된다.

